Det afterload svarer til modstanden, der virker mod sammentrækningen af hjertemuskelen og begrænser således udstødningen af blod fra hjertet. Efterbelastningen af hjertet øges for eksempel i forbindelse med hypertension eller ventilstenose. For at kompensere for dette kan hjertemuskelen hypertrofi og fremme hjertesvigt.
Hvad er bagladningen?

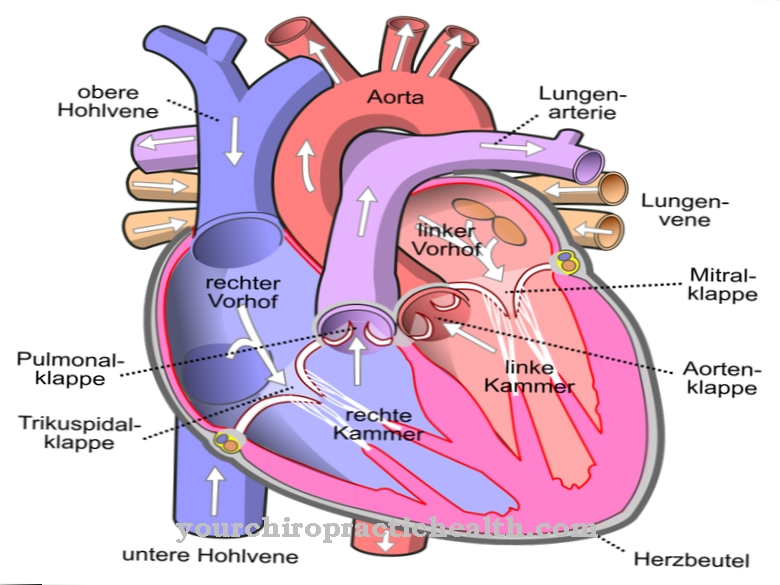
Hjertet er en muskel, der pumper blod ind i blodomløbet gennem skiftevis sammentrækning og afslapning og dermed er involveret i tilførslen af næringsstoffer, budbringere og ilt til kroppens væv.
For at begrænse udkastet af blod fra hjertekamrene modvirker den såkaldte efterbelastning sammentrækningen af hjertekamrene. Alle kræfter, der modsætter sig udstødning af blod fra hjertekammerne ind i blodkarsystemet, opsummeres som efterbelastning. Ventrikulært myokard har en vis vægspænding. Vægspændingen i begyndelsen af systolen (blodudkastningsfase) skal forstås som hjernens efterbelastning under fysiologiske forhold. I en sund krop overvinder det ventrikulære myokardiums vægspænding det end-diastoliske aorta-tryk eller lungetrykket og starter således udkastningsfasen.
Efterbelastningen med hensyn til vægspænding når sit maksimum kort efter åbningen af aortaventilen.
Værdien af efterbelastningen bestemmes af både det arterielle blodtryk og arteriernes stivhed. Sidstnævnte faktor er også kendt som compliance. Forbelastningen skal adskilles fra efterbelastningen. Det svarer til alle de kræfter, der strækker de kontraktile muskelfibre i hjerteventriklerne mod slutningen af diastolen (afslapningsfasen af hjertemuskelen).
Funktion & opgave
Efterbelastning er den modstand, som venstre ventrikel skal overvinde kort efter, at aortaventilen åbner for at udvise blod fra hjertet. Vægspændingen i begyndelsen af systolen regulerer blodudkastet. I medicin er systole hjertets sammentrækningsfase. Den ventrikulære systole består af en spændingsfase og en udvisningsfase (også kendt som udvisningsfase). Systolen tjener således til at sprøjte blod fra atriet ind i hjertekammeret eller fra kammeret ind i det vaskulære system. Hjertets pumpekapacitet afhænger derfor af systolen, hvor to systoler hver afbrydes af en diastol. Systolen er omkring 400 ms ved en frekvens på ca. 60 / min.
Modstanden, der skal overvindes i blodets uddrivningsfase, er efterbelastningen, hvorved kraften til systolen afhænger af ventrikelvolumenet i sammenhæng med den såkaldte Frank-Starling-mekanisme. Hjerteslagsvolumen er også resultatet af den perifere modstand. Frank Starling-mekanismen svarer til forholdet mellem fyldning og udstødning af hjertet, der tilpasser hjertets aktivitet til kortvarigt pres og volumenudsving og tillader begge hjertekamre at skubbe den samme slagvolumen ud.
Hvis forbelastningen for eksempel øges, hvilket resulterer i et forøget slutdiastolisk fyldvolumen af ventriklen, forskyver Frank-Starling-mekanismen referencepunktet på afslapningskurven mod højre. Så kurven for den maksimale støtte forskydes til højre. Den øgede fyldning giver mulighed for større isobariske og isovolumetriske maksima. Det udsatte slagvolumen øges, og det slut-systoliske volumen stiger lidt.
En stigning i forbelastningen øger hjertets tryk-volumen arbejde. Efterbelastningen øges. Denne øgede modstand mod udkast afhænger af det gennemsnitlige aortatryk. Med øget efterbelastning skal hjertet opnå et højere tryk op til åbningen af lommeventilen i spændingsfasen. På grund af den øgede sammentrækningskraft falder slagvolumen og slut-systolisk volumen. Samtidig stiger det slutdiastoliske volumen. Den efterfølgende sammentrækning øger igen forladningen.
Sygdomme og lidelser
Klinisk bruges blodtryk normalt til at estimere efterbelastningen eller vægspændingen. Bestemmelsen af blodtrykket i begyndelsen af udvisningsfasen på myokardiet (hjertemuskelen) tillader kun en tilnærmelse til de faktiske efterbelastningsværdier. Den nøjagtige bestemmelse af impedansen er ikke mulig. Efterbelastningen i daglig klinisk praksis estimeres også tilnærmelsesvis ved hjælp af transesophageal ekkokardiografi.
Ved hjerteinsufficiens er den systoliske kraft i hjertemuskelen ikke længere relateret til det diastoliske fyldvolumen efter behov. Som et resultat reagerer blodtrykket ikke længere passende på stressede situationer. Dette fænomen karakteriserer oprindeligt træningsafhængig hjerteinsufficiens, som over tid kan blive hvilemangel. I tilfælde af udtalt hjertesvigt er det ikke længere muligt at opretholde blodtryk i hvile, og hjertrelateret hypotension sætter sig ind, dvs. et tab af tone. I modsætning hertil øger hypertension i betydningen øget tone efterbelastningen. Hjertet skal øge sin udsprøjtningsevne med en sådan stigning i tone, men opfylder kun dette krav i det omfang, dets strømudviklingsmuligheder er tilstrækkelige. Ved koronar hjertesygdomme modvirker iltforsyningen og ved kardiomyopati muskelstyrken dette aspekt som en begrænsende faktor. For høj efterspørgsel ledsager adskillige hjertesygdomme.
Efterbelastningsstigningen kan reguleres til en vis grad med medicin. AT1-blokkeringer betragtes for eksempel som terapeutiske reduktioner efter belastning. ACE-hæmmere, diuretika og nitroglycerin reducerer både forbelastningen og efterbelastningen. Derudover kan arterielle vasodilatorer, såsom calciumantagonister af dihydropyridintypen, sænke hjerteets efterbelastning. Vasodilatorer slapper af de vaskulære muskler og forstørrer karens lumen. ACE-hæmmere sænker på sin side blodtrykket, hvilket reducerer efterbelastningen af hjertets arbejde. Derfor bruges de ofte til behandling af hjertesvigt, men bruges også ved koronar hjertesygdom. AT1-blokkere er konkurrencebegrænsende hæmmere og virker selektivt på den såkaldte AT1-receptor, hvor de modvirker den kardiovaskulære effekt af angiotensin II. Frem for alt sænker de blodtrykket og reducerer efterbelastningen i overensstemmelse hermed.
Efterbelastningen øges ikke kun gennem hypertension, men også i forbindelse med ventilstenose. I henhold til Laplace's lov øges den ventrikulære muskulatur for at kompensere for en kronisk forøget efterbelastning for at modregulere og reducere den øgede vægspænding. Som et resultat kan den berørte ventrikel udvides, hvilket igen fører til hjertesvigt.



.jpg)





.jpg)



.jpg)