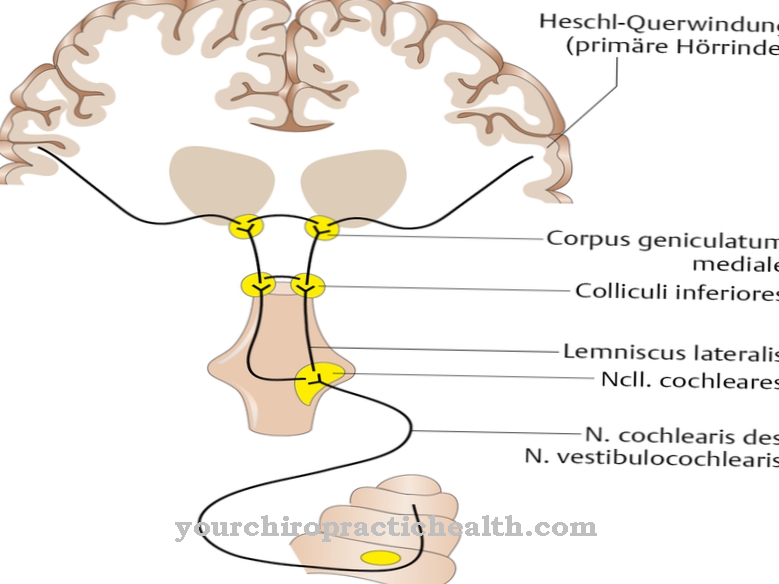
Dræberceller er en del af immunsystemet. Som såkaldte cytotoksiske T-celler (erhvervet immunsystem) eller som naturlige dræberceller (medfødt immunsystem) genkender de og angriber celler, der er fremmed for kroppen og ændrede kropsceller, såsom kræftceller, celler inficeret med vira eller bakterier eller ældende celler. Dræbercellerne frigiver stoffer, der delvist perforerer cellemembranen i de angrebne celler, så programmeret celledød eller apoptose sættes i bevægelse.
Hvad er en dræbercelle?
Dræberceller er en vigtig del af immunsystemet. De genkender strukturer, der er fremmed for kroppen og ændrede kroppens egne celler, for eksempel celler inficeret med vira eller bakterier og celler, der er degenereret i kræftceller.
To forskellige typer dræberceller kan genkendes, de såkaldte naturlige dræberceller (NK-celler), som er en del af det medfødte immunsystem, og de cytotoksiske T-celler, der er en del af det adaptive eller adaptive immunsystem. For at skelne mellem ven og fjende fungerer de to celletyper med forskellige systemer. NK-celler har visse receptorer, der er placeret i deres plasmamembran og interagerer med såkaldte MHC-I-molekyler (Major Histocompatibility Complex), der viser sunde endogene celler på deres overflade.
Hvis MHC-I-molekylerne er fraværende, eller visse molekyler mangler - som normalt er tilfældet med kræftceller eller celler inficeret med vira, aktiveres disse. Mens NK-celler fungerer uspecifikt, er de cytotoksiske T-celler karakteriseret ved ekstrem specificitet. I inficerede kropsceller viser MHC-I-komplekserne også andre peptider eller andre specifikke stoffer, såkaldte antigener. Cytotoksiske T-celler er hver især specialiserede i at genkende et specifikt antigen.
Anatomi & struktur
NK-celler har deres oprindelse i lymfatiske forløberceller, der udvikler sig i knoglemarven og frigøres efter differentiering i blodet og lymfesystemerne. Som et våben mod celler, der skal dræbes, er der adskillige lysosomer i deres cytoplasma, der vendes, når NK-cellen aktiveres, så det cytotoksiske stof, der er placeret i lysosomerne, frigøres og målcellen lyseres.
Et vigtigt anatomisk træk er to forskellige typer receptorer på deres overflade. De hæmmer og aktiverer receptorer, der reagerer med MHC-I-molekylerne, præsenterer målcellerne på deres overflade og aktiverer eller inaktiverer NK-cellerne. Cytotoksiske T-celler stammer også fra knoglemarven, men for deres differentiering tager de omvejen via thymus, som har givet dem navnet T-celler.
I thymusen differentieres cellerne i T-celler og modtager deres specifikke T-cellereceptor, før de også frigøres i blodbanen. Deres specifikke receptor består af et proteinkompleks, som de bærer på deres overflade og genkender specifikke antigener, der præsenteres for målcellerne sammen med MHC-I-molekylerne.
Funktion & opgaver
Killercellernes hovedopgave er identifikation og øjeblikkelig ødelæggelse af inficerede celler og degenererede tumorceller med vira eller andre intracellulære patogener. De to forskellige typer dræberceller, NK-celler og de cytotoksiske T-celler, er tilgængelige for at udføre opgaven. De evolutionært meget ældre NK-celler har evnen til at kontrollere "ID-kort" for målcellerne og deres MHC-I-molekyler for tilstedeværelse og fuldstændighed. Hvis NK-celler støder på celler med ufuldstændige MHC-I-molekyler eller celler uden genkendelige MHC-I-molekyler, angriber NK-cellerne øjeblikkeligt.
De frigiver stoffer, der lyser cellemembranen af de angrebne celler. I den angrebne celle udløses apoptose normalt, programmeret celledød, som inkluderer en slags selvdestruktion med definerede fragmenter, som stort set genindføres i den mellemliggende stofskifte. Makrofager fagocytter derefter resterne og transporterer dem væk. De evolutionært meget mere "moderne" cytotoksiske dræberceller er kun specialiseret i et bestemt antigen via deres specifikke receptorer, så de genkender ikke andre antigener, men har flere muligheder i tilfælde af deres aktivering.
De kan modnes til T-hjælperceller eller cytotoksiske T-celler med høj hastighed og blive aktive i overensstemmelse hermed. De frigiver perforiner for at lysere målcellens membran og granzymer, der udløser apoptose. Derudover udskiller de interleukiner og interferoner, regulatoriske peptider, der kontrollerer immunresponset mod en virusinfektion.Da en cytotoksisk T-celle kun kan genkende “dets” specifikke antigen, skal thymusen fremstille cytotoksiske T-celler for hver type antigen, hvoraf der sandsynligvis er flere millioner.
Fordelen ved specialisering er, at immunsystemet kan tilpasse sig nye krav, f.eks. B. på kontinuerligt modificerede vira kan justeres. Der er praktisk taget en konstant race mellem det adaptive immunsystem og de genetisk ændrende vira. For ikke konstant at skulle beholde et stort reservoir af hver T-celle, der produceres, producerer thymusen langlivede hukommelsesceller, der tjener som grundlag for at bekæmpe fornyet infektion med det tilsvarende patogen og gøre immunresponset 100 gange hurtigere.
Du kan finde din medicin her
➔ Medicin til styrkelse af forsvaret og immunforsvaretsygdomme
Arbejdet med dræbercellerne er meget dynamisk og er også underlagt hormonel kontrol. F.eks. Fører en akut stressbegivenhed til en øget spredning af NK-celler og øget årvågenhed, så at sige til den røde alarm.
De specifikt effektive cytotoksiske T-celler bremses, fordi de næppe kunne give et nyttigt bidrag under en akut situation, der kræver hurtige reaktioner. I tilfælde af kronisk stress er imidlertid hele immunsystemet svækket. Alle typer dræberceller falder i antal og i deres årvågenhed, så modtageligheden for infektion øges.
En af de vigtigste sygdomme i forbindelse med cytotoksiske T-celler er autoimmune sygdomme, hvor dræbercellerne ikke genkender kroppens egne celler som sådan, men angriber dem og producerer tilsvarende autoimmune antistoffer. Mekanismen til udvikling af autoimmune sygdomme er endnu ikke fuldt ud forstået. Det accepteres generelt, at genetiske faktorer i det mindste spiller en gunstig rolle her.





.jpg)



.jpg)