Det Joubert syndrom er kendetegnet ved en medfødt misdannelse af hjernestammen såvel som en agenese (inhiberingsmisdannelse, manglende tilknytning, for eksempel hjernestænger, appendiks). Hypoplasia (underudvikling) af cerebellar ormen kan også eksistere. Patienter, der lider af denne autosomale recessive genetiske defekter, viser blandt andet unormal vejrtrækningsadfærd og ataksi.
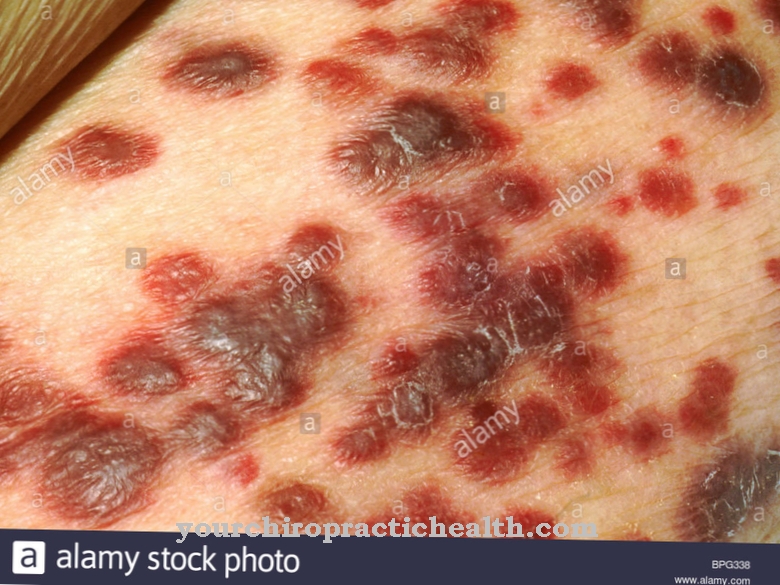
Hvad er Joubert syndrom?

© Sashkin - stock.adobe.com
Mennesker med Joubert syndrom lider af udviklingsforstyrrelser i centralnervesystemet og de deraf følgende funktionelle forstyrrelser. Medicinsk forskning er kontroversiel om, hvorvidt denne genetiske lidelse skal klassificeres som en sygdom i sig selv.
De berørte patienter har en række forskellige symptomer. På grund af dette er en endelig diagnose vanskelig. JB er kendetegnet ved omfattende genlokus heterogenitet. Indtil videre er der identificeret flere genmutationer. En mutationsanalyse er meget omfattende.
årsager
Joubert syndrom hører til gruppen af primære ciliophatias. Med denne genetiske forstyrrelse i den primære cilie eller i basallegemet kan forskellige typer udviklingsforstyrrelser forekomme. Som særlige celleprocesser udfører cilia forskellige opgaver. De fungerer som kemo-, mechano- og osmosesensorer og er involveret i mange signalveje. Desuden sikrer de normal organudvikling.
De opretholder vævshomeostase i de grundlæggende udviklingsprocesser. Et stort antal af de involverede proteiner danner et komplekst netværk gennem interaktion. Hvis andre organer påvirkes ud over de vigtigste symptomer, er JSRD (Joubert Syndrome Related Disorder) til stede. Denne sekundære sygdom er kendetegnet ved yderligere organ manifestationer, der involverer nyrer, lever og øjne.
Det er et genetisk heterogent syndrom. Læger har fundet misdannelser i NPHP6 / CEP290-genet (kodende for nephrocystine-6) eller i NPHP8 / RPGRIP1L-genet (kodende for nephrocystine-8). Andre genmutationer er MKS3, ARL13B, AHI1, CC2DA2, TMEM216 og INPP5E. Kun få patienter har mutationer i NPHP4 og NPHP1.
Symptomer, lidelser og tegn
Det patognomoniske træk er det "molære tandskilte" (MTS), som kan bestemmes ved anvendelse af "aksial T1-vægtet magnetisk resonansafbildning i hjernen". Dette træk er kendetegnet ved agenese eller hypoplasi af cerebellar ormen eller cerebellar ormen. Endvidere trækkes den bageste, vinkelrette fossa (pit mellem cerebralbenene) stærkt ind, og de cerebellare stængler har en fremtrædende overlegen form på grund af en misdannelse af mellemhovedet.
Ud over MTS lider patienter ofte af åndedrætsforstyrrelser, ataksi, muskelhypotension og psykomotorisk retardering. 8 til 19 procent af de berørte viser postaxial polydactyly (flere fingre) og seks procent har occipital (meningo) encephalocele, hvor bagsiden af hjernen svulmer ud.
Denne deformitet blev første gang registreret i 1969. Forekomsten er cirka 1: 100.000, et forhold, der viser, hvor sjældent sygdommen forekommer. Der er kun dokumenteret hundrede tilfælde siden den første medicinske undersøgelse. Da denne genetiske defekt forekommer i forskellige former og varianter, antager læger adskillige ændringer i genetik.
En nøjagtig afvigelse er endnu ikke blevet bekræftet endeligt. Imidlertid betragtes en mutation af X-kromosomet som sikker. Denne lidelse overføres på grundlag af autosomal recessiv arv. En manglende vermis cerebelli (cerebellum, cerebellar orm), skade på nethinden og en mærkbar iris er involveret.
Ofte forekommende symptomer og klager i den nyfødte periode er nystagmus og et uregelmæssigt åndedrætsmønster som episodisk tachypnea og apnø. Små børn kan udvikle hypotoni. Med udviklingen af alder udvikles ubalance og en ujævn gang (ataksi). Disse vigtigste symptomer er også kendt som motoriske milepæle.
Patienterne har forskellige niveauer af kognitive evner og kan være alvorligt nedsat, men de kan også vise et normalt niveau af intelligens. Oculo-motor apraxia (bevægelsesforstyrrelse) er også mulig.
Karakteristisk for denne genetiske defekt er kraniofaciale abnormiteter, såsom et stort hoved, afrundede og høje øjenbryn, en fremtrædende (udstikker) pande, en deformeret mund, en rytmisk bevægende og udstående tunge og dybde ører. Lejlighedsvise symptomer er nefrophthisis, retinal dystrofi og polydactyly.
Diagnose & sygdomsforløb
En diagnose stilles på baggrund af de tidligere citerede karakteristiske milepæle for ataksi, hypotension, oculomotor apraxia, åben vermis cerebelli efter den 18. uge af graviditeten og udviklingsforsinkelse. Derudover foretages et karakteristisk neuroradiologisk fund i MRI, MTS (molært tandskilt).
Denne funktion, kendt som det molære tegn, skyldes misdannelser i suget og mellemhovedet samt hypoplasien i den lille hjerneorm. Differentialdiagnoser stilles på grundlag af sygdomme, der er tæt beslægtet med JS, såsom JSRD (Joubert syndrom-relateret lidelse), Dandy-Walker-misdannelse (misdannet cerebellar orm uden MTS), typer 1 og 2 af oculomotor apraxia, ponto-cerebral hypoplasia og atrofi, 3-c Syndrom, orofacio-digitale syndromer II og III samt Meckel-Gruber syndrom.
Fase I inkluderer den "næste generations sekvensbestemte panelanalyse" af generne JBTS5 (53 kodende eksoner), JBTS3 (26 kodende eksoner), JBTS6 (28 kodende eksoner) og JBTS9 (36 kodende eksoner). JBTS4-genet testes for homozygot deletion ved multiplex PCR. I trin II analyseres de andre JB-gener ved hjælp af PCR (en proces, der duplikerer gensekvenser i DNA-kæden afhængigt af enzymet) og efterfølgende Sanger-sekventering, afhængigt af fænotype træk, svarende til faldende mutationsfrekvenser.
For at udelukke kromosomale ubalancer udføres den differentielle diagnostiske SNP-array-analyse. Hvis der er en forbløffelse, eller hvis der er kendt flere syge personer i familien, foretager lægerne homozygositetsscreening ved hjælp af koblingsanalyse i mikrosatellitmarkøren, der flankerer genet og efterfølgende genanalyse ved hjælp af Sanger-sekventering. To til ti milliliter EDTA-blod tages fra børn som diagnostisk materiale; fra voksne er mængden fra fem til ti milliliter.
DNA eller vævsmateriale er også egnet. Fase I: Genomisk DNA-materiale undersøges for eksistensen af duplikationer eller deletioner ved hjælp af en kvantitativ analyse af NPHP1-genet under anvendelse af MLPA. Meget små mængder DNA i genomet undersøges for deletioner og duplikationer af individuelle eksoner (gensegmenter). Fase II: De kodede eksoner af de hidtil identificerede gener evalueres ved hjælp af næste generations frekvenser. Splejsningsstederne er beriget ved sondehybridisering.
Komplikationer
Joubert syndrom får de fleste patienter til at lide af forskellige lidelser. Dette fører normalt til kort statur, åndedrætsforstyrrelser og desuden til forsinkelse. Barnets mentale udvikling kan også begrænses. Åndedrætsvanskelighederne kan også føre til åndenød, som bestemt skal behandles.
Det er ikke ualmindeligt, at personens forældre lider af svær depression eller andre psykologiske lidelser. Patienterne viser også balanceforstyrrelser og lider ofte af begrænset mobilitet. Det er ikke ualmindeligt for ubehag for øjne og ører, hvilket fører til høretab eller synsproblemer. Patientens livskvalitet reduceres markant af Joubert syndrom.
Ved hjælp af forskellige behandlingsformer kan Joubert syndrom begrænses og behandles. Desværre kan en årsagsbehandling ikke udføres. I nødsituationer kan nødventilation også udføres, hvis der er åndenød. Der er ingen særlige komplikationer i selve behandlingen. Generelt kan det ikke forudsiges, om patientens forventede levetid vil blive reduceret med Joubert syndrom.
Hvornår skal du gå til lægen?
En vordende mor bør deltage i alle tilgængelige kontrolundersøgelser under graviditeten. I undersøgelserne undersøges gravidens helbredstilstand såvel som det ufødte barns helbredstilstand. Da Joubert syndrom kan diagnosticeres allerede i den 18. uge af graviditeten, anbefales det at gøre brug af den forebyggende medicinske kontrol, som sundhedsforsikringsselskaberne anbefaler. Derudover anbefales genetisk rådgivning og undersøgelse, hvis der er en genetisk defekt i forældrenes historie.
I det usandsynlige tilfælde, at der ikke blev konstateret nogen uregelmæssighed i livmoderen, foregår automatisk kontrol af fødselslæger og børnelæger umiddelbart efter fødslen. Åndedrætsforstyrrelser kan påvises under disse undersøgelser. Hvis barnets forældre bemærker usædvanlige uoverensstemmelser, der tidligere ikke er blevet opdaget, skal observationerne drøftes med en læge. Hvis der er fysiske særegenheder, korte staturer eller misdannelser, skal en læge konsulteres.
Hvis man i direkte sammenligning med børn i samme alder bemærker sprogproblemer eller mental underudvikling, skal man konsultere en læge. Undersøgelser er nødvendige for at afklare årsagen. Jo hurtigere der stilles en diagnose, kan de tidligere målrettede behandlinger initieres for at støtte barnet. Konsultation med en læge bør derfor foretages ved det første tegn på en unormalitet.
Behandling og terapi
Forældrene har ret til genetisk rådgivning. Behandlingsmulighederne er lige så forskellige som årsagerne til denne sygdom er forskellige. I tilfælde af motoriske udviklingsforstyrrelser og hypotension, spiller uddannelsesmæssige støtteprogrammer, sprog, ergoterapi og ergoterapi, som kan have en gavnlig virkning på sygdomsforløbet.
Dem, der er berørt med unormale åndedrætsmønstre, kan også få ilterstatning eller ventilation. Patienter med milde symptomer har en positiv prognose. Patienter, der er hårdt ramt, skal plejes af et ekspertreferencecenter.
Outlook og prognose
Prognosen for Joubert syndrom er dårlig. Dette syndrom er en genetisk lidelse. Med de nuværende medicinske, videnskabelige og juridiske krav kan dette ikke helbredes. Forskere og læger har lovligt ikke lov til at ændre en persons genetiske forhold gennem interventioner. Af denne grund er behandlingen rettet mod brugen af terapier, der skal forbedre den eksisterende livskvalitet. Uden brug af medicinsk behandling reduceres patientens reducerede velvære yderligere.
Jo tidligere syndromet kan diagnosticeres og behandles, jo bedre bliver resultaterne. I nødsituationer angives nødventilation af den pågældende, ellers kan patienten dø for tidligt. Selvom adskillige behandlingsformer sammensættes og anvendes i en individuel behandlingsplan, kan den eksisterende sygdom føre til sekundære lidelser. Disse forværrer den samlede prognose.
Eksisterende funktionsforstyrrelser eller andre bevægelsesbegrænsninger kan føre til psykiske sygdomme. Midlertidig eller vedvarende depression, humørsvingninger eller ændringer i personlighed er dokumenteret hos mange patienter. Dette repræsenterer en ekstra byrde for den pågældende og miljøet. Hverdagen for en patient med Joubert-syndrom kan ofte kun styres med tilstrækkelig hjælp og støtte fra pårørende. Balanceforstyrrelser og ataksi bliver mere alvorlige med alderen.
forebyggelse
Da en nøjagtig genetisk årsag endnu ikke er blevet endeligt fastlagt, er der ingen forebyggende foranstaltninger i klinisk forstand. Den eneste måde at modvirke misdannelser i den menneskelige organisme er at føre en sund livsstil.
Efterbehandling
I de fleste tilfælde har patienten med Joubert-syndrom ingen direkte eller specielle opfølgningsmuligheder, således at den berørte person primært er afhængig af en hurtig og frem for alt tidlig diagnose af sygdommen. Jo tidligere sygdommen genkendes, jo bedre er det videre kurs. Det anbefales derfor at kontakte en læge ved de første symptomer og tegn.
Med denne sygdom er den berørte normalt afhængig af intensiv pleje og terapi, der kan lindre symptomerne. Hjælp og støtte fra forældre og nære slægtninge er også meget efterspurgt for at gøre det muligt for den berørte at leve et normalt liv som muligt. Ofte kan øvelserne fra fysioterapi eller fysioterapi også udføres i dit eget hjem, hvilket kan lindre symptomerne.
Symptomerne kan ikke altid lindres fuldstændigt. Kontakt med andre patienter af Joubert syndrom kan også være meget nyttigt, da det ikke er ualmindeligt at udveksle information. Som regel reduceres den forventede levetid ikke af denne sygdom.
Du kan gøre det selv
Joubert syndrom er uhelbredelig, og hverdagens hjælp er også vanskelig. Symptomerne på den medfødte sygdom er i de fleste tilfælde uundgåelige. Det er stadig muligt, at nogle af dem bliver afhjulpet.
Da vejrtrækning er særlig forstyrret hos de berørte, er dette et udgangspunkt. Et optimeret rumklima kan være nyttigt. Tør varmeluft kan forværre vejrtrækningsproblemer. Luft, der er for kold, har samme effekt. Ideelt set er stuetemperaturen omkring 20 ° C og fugtigheden omkring 50 procent. Især indendørs planter kan bidrage til et optimalt indeklima. Alternativt kan fugtige håndklæder også placeres i rummet for at holde fugtigheden på det ønskede niveau. Indeklimaet kan spores ved hjælp af et hygrometer. Et andet udgangspunkt, der også målretter vejrtrækning, er vejrtrækningsøvelser. Regelmæssig brug forbedrer opfattelsen af den ellers automatiske proces. På denne måde kan du forhindre vejrtrækning for hurtigt og åndedrætspauser.
Det giver også mening, hvis de berørte ikke sover alene i et rum. Pårørende kan opleve pauser i vejrtrækningen under søvnen og vække patienten eller stimulere dem til at trække vejret. Men det er bare en forholdsregel.


.jpg)













.jpg)