Phenylalanin er en proteinogen, essentiel aminosyre med en aromatisk seks-leddet ring, der fungerer som en byggesten for mange proteiner og peptider.
Phenylalanin spiller også en vigtig rolle i nitrogenmetabolismen og kan omdannes i leveren til den proteinogene aminosyre-tyrosin. Phenylalanin og tyrosin spiller en vigtig rolle i syntesen af insulin, melanin, thyroxin og neurotransmittorer dopamin, serotonin og tyramin.
Hvad er phenylalanin?
Phenylalanin er en essentiel alfa-aminosyre, der - i modsætning til de fleste proteinogene aminosyrer - ikke kun er bioaktiv i L-formen, men i begrænset omfang også som en enantiomer i R-formen.
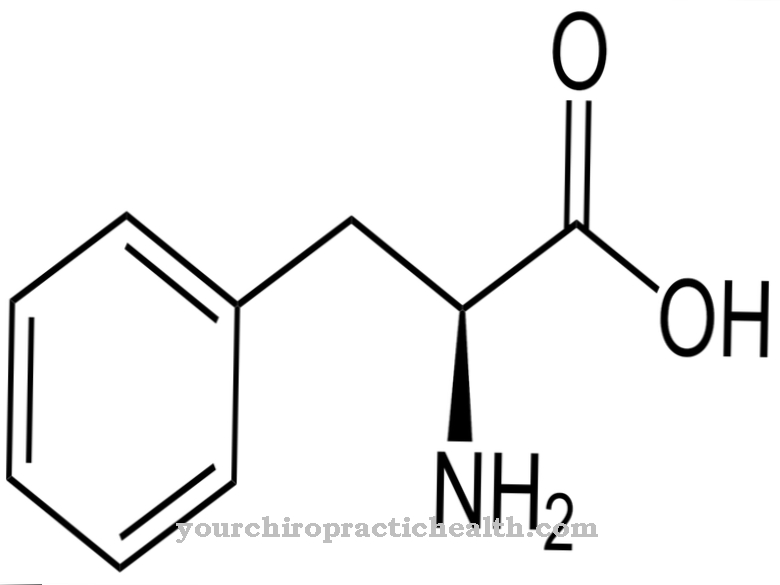
R-phenylalanin er biokemisk stort set inaktiv og forekommer udelukkende under den kunstige produktion af aminosyren, men D-phenylalanins rolle i kontrollen af visse neurotransmittere i smertekomplekset diskuteres. Som et karakteristisk strukturelt træk har phenylalanin en simpel aromatisk seks-leddet ring (benzenring) med en fastgjort carbonhydridkæde. Den kemiske strukturformel er C6H5-CH2-CH (NH2) -COOH, hvor C6H5-gruppen angiver benzenringen. Aminosyren er amfifil, hvilket betyder, at den er både fedt og vandopløselig.
Den kemiske formel viser også, at phenylalanin udelukkende består af kulstof, brint, nitrogen og ilt, stoffer, der er allestedsnærværende. Sjældne metaller, mineraler eller sporstoffer er ikke en del af aminosyren. Ikke desto mindre kan den menneskelige metabolisme ikke syntetisere phenylalanin i tilstrækkelig grad fra tyrosin, men er afhængig af indtagelse fra mad. Phenylalanin findes i tilstrækkelige mængder i mange dyre- og vegetabilske fødevarer, så der ikke er behov for at frygte en mangel på aminosyren i en normal, blandet diæt - forudsat at fordøjelseskanalen normalt absorberes.
Funktion, effekt og opgaver
Phenylalanins vigtigste funktion og opgave er at deltage i strukturen af mange proteiner og peptider. Det er også involveret i syntesen af nogle hormoner, der spiller en central rolle i styringen af metaboliske processer.
Der er hormoner som adrenalin, norepinephrin, L-dopa, PEA og melanin. Derudover fungerer L-phenylalanin som det basale stof, hvorfra z. B. messenger-stoffet dopamin, serotonin, tyramin og andre kan syntetiseres. L-phenylalanin tjener også som udgangsmateriale til den essentielle aminosyretyrosin. Til dette formål omdannes phenylalanin til tyrosin i leveren i to trin ved hydroxylering og ved opdeling af et vandmolekyle. Phenylalaninhydroxylase er det enzym, der katalyserer omdannelsen til tyrosin.
En alternativ forsyning af den også essentielle aminosyre-tyrosin kan - som med phenylalanin - finde sted gennem madindtag. I modsætning til alle andre aminosyrer, der kun viser bioaktive effekter i deres L-form, synes D-enantiomeren af fenylalanin i det mindste at have indflydelse på opfattelsen af smerte. En blanding af L- og D-phenylalanin (racemisk blanding) viste sig at have en smertestillende virkning. DL-blandingen blokerer sandsynligvis for nedbrydningen af enkephaliner - kroppens egne opioider - så den smertestillende effekt forlænges og intensiveres.
Uddannelse, forekomst, egenskaber & optimale værdier
Den essentielle aminosyre, phenylalanin, absorberes gennem mad. Det er ikke frit, men normalt som en del af et protein eller polypeptid i kemisk bundet form. For at gøre aminosyren tilgængelig for metabolismen skal det tilsvarende protein først nedbrydes i løbet af fordøjelsen og derefter ekstraheres fra "fragmenterne" under anvendelse af yderligere enzymer i den yderligere metabolisme.
L-phenylalanin syntetiseres via den såkaldte shikiminsyrevej. Det er en kompleks biokatalytisk kædereaktion, som autotrofiske planter og bakterier har. Det særlige ved autotrofiske organismer er deres evne til at danne organisk stof udelukkende fra uorganisk materiale. Gratis L-phenylalanin smager bittert, mens dens D-enantiomer, der udelukkende produceres i industriel produktion, har en sød smag. Aminosyren er z. B. tilbydes som et kosttilskud og er også en del af det kunstige sødestof aspartam. Biotilgængelig L-phenylalanin findes i bunden form i mange fødevarer.
Deres indhold er især højt i tørrede ærter og sojabønner, i valnødder og græskarfrø samt i forskellige typer fisk og kød. Phenylalaninbehovet er stærkt afhængigt af forsyningen med tyrosin. Hvis der ikke er tyrosin i kosten, har kroppen brug for 38 til 52 mg pr. Kg kropsmasse. Med en rig forsyning med tyrosin i kosten falder det daglige behov til kun 9 mg pr. Kg kropsmasse. Som regel indeholder fødevarer, der indeholder fenylalanin, også en tilsvarende mængde tyrosin.
FAO / WHO's anbefaling fra 1985 udgør et samlet krav til L-phenylalanin og L-tyrosin på 14 mg pr. Kg kropsmasse pr. Dag. En voksen med 80 kg kropsmasse har derfor brug for 1.120 mg af de to stoffer dagligt.
Sygdomme og lidelser
Symptomer på mangel i tilfælde af en permanent utilstrækkelig forsyning af phenylalanin og tyrosin i kosten er ekstremt sjældne, men kan have alvorlige konsekvenser, især i det neuronale område.
Bortset fra en forringelse af syntesen af mange hormoner og neurotransmittorer, kan manglen også manifesteres ved en forstyrrelse i myeliniseringen af nervefibre. Det modsatte af en mangel, en overkoncentration af phenylalanin (phenylketonuria), kan forekomme på grund af en genetisk metabolisk lidelse. Sygdommen arves på en autosomal recessiv måde og fører til en reduceret produktion af enzymet fenylalaninhydroxylase, som kan omdanne phenylalanin til tyrosin.
Den reducerede enzymaktivitet fører til en stærk stigning i aminosyren, til det, der er kendt som fenylketonuri, fordi omdannelsen til tyrosin også er nedbrydningsvejen for phenylalanin. På samme tid er der en mangel på tyrosin, fordi syntesevejen er blokeret. En anden arvelig sygdom i denne sammenhæng er Hartnup syndrom. Det er en metabolisk lidelse, der forstyrrer transporten af phenyalanin over cellemembranen. Dette fører til alvorlige problemer i CNS, på huden og fordøjelseskanalen.

.jpg)

.jpg)

.jpg)