Som en del af Genterapi Gener til behandling af genetiske sygdomme indsættes i et humant genom. Som regel anvendes genterapi til udtalt sygdomme, såsom SCID eller septisk granulomatose, som ikke kan kontrolleres ved konventionelle terapeutiske fremgangsmåder.
Hvad er genterapi?

Som Genterapi er det udtryk, der bruges til at beskrive indsættelsen af gener eller genomsegmenter i humane celler. Det sigter mod at kompensere for en genetisk defekt til behandling af arvelige sygdomme.
Generelt kan der sondres mellem somatisk genterapi og kimlineterapi. Ved somatisk genterapi ændres kroppens celler på en sådan måde, at kun det genetiske materiale i cellerne i det kropsvæv, der skal behandles specifikt, modificeres. De ændrede genetiske oplysninger overføres derfor ikke til næste generation.
I forbindelse med kimlineterapi, der er forbudt i næsten alle lande, er der en ændring i den genetiske information i kimlinjens celler. Afhængigt af den terapeutiske strategi sondres der desuden mellem substitutionsbehandling (udveksling af defekte genomsegmenter), addisjonsbehandling (forstærkning af specifikke genfunktioner såsom immunforsvar i kræft eller infektionssygdomme) og undertrykkelse terapi (inaktivering af patogene genaktiviteter).
Da gensekvensen kan indsættes permanent eller midlertidigt i målcellen, kan effekten af en genterapi også være permanent eller midlertidig.
Funktion, effekt & mål
Generelt sigter man Genterapi Ved at udskifte det defekte med et intakt gen er målcellen i stand til at syntetisere stoffer, der er essentielle for organismen (inklusive proteiner, enzymer).
Substitutionen af det genetiske materiale kan udføres uden for kroppen (ex vivo). Til dette formål fjernes cellerne, der har den defekt, der skal behandles, fra den berørte person og udstyres med et intakt gen. De modificerede celler returneres derefter til den berørte person. Gentransporten ind i cellen kan sikres ved forskellige metoder.
I såkaldt kemisk transfektion påvirker en elektrisk forbindelse cellemembranen, så det terapeutiske gen kan komme ind i cellen. Det modificerede genetiske materiale kan fysisk komme ind i celleindretningen gennem en mikroinjektion eller en elektrisk impuls, der får cellemembranen midlertidigt til at permeatere (elektroporation). Derudover kan de ændrede oplysninger skydes ind i cellen på små guldkugler (partikelpistol).
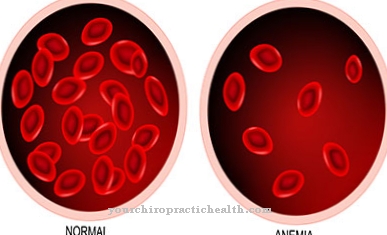
Som en del af en transfektion ved anvendelse af erythrocyt-spøgelser lyseres erythrocytter (røde blodlegemer) med de terapeutiske gener i en opløsning. Som et resultat åbnes cellemembranerne kortvarigt, og gensekvensen kan trænge ind. De ændrede erythrocytter smeltes derefter sammen med målcellerne.
Derudover kan genetisk modificerede virusser injiceres gennem det, der kaldes transduktion. Da vira afhænger af en værts metabolisme for at formere sig, kan de fungere som såkaldte genbusser ved at smugle det nye, sunde genetiske materiale ind i målcellerne. DNA, RNA og især retrovira anvendes til transduktionsprocessen. Egnede målceller inkluderer leverceller, T-celler (T-lymfocytter) og knoglemarvsceller.
Genterapi anvendes hovedsageligt til svære immunsystemsygdomme, såsom SCID (defekte T-lymfocytter) eller septisk granulomatose (defekte neutrofile granulocytter). Det repræsenterer også en mulig alternativ terapi for tumorer, alvorlige infektionssygdomme såsom HIV, hepatitis B og C, tuberkulose eller malaria, hvorved de terapeutiske muligheder, især med hensyn til HIV og tuberkulose, stadig undersøges klinisk.
Den genterapeutiske transduktion med retrovira på kroppens egne blodstamceller er især egnet til beta-thallassæmi (nedsat betaglobinsyntese).
Risici, bivirkninger og farer
Mens få sygdomme er forårsaget af a Genterapi kan behandles, dog kan risikoen ikke vurderes fuldt ud i mange tilfælde på grund af det lave udviklingsniveau af terapien.
Den største risiko i genterapi ligger i den hidtil ikke styrede integration af den terapeutiske gensekvens i målcellen. I tilfælde af forkert integration i genomcellen til målcellen kan funktionen af intakte gensekvenser forringes, og andre alvorlige sygdomme kan udløses. For eksempel kan proto-oncogener, der støder op til det indsatte gen, aktiveres, hvilket nedsætter normal cellevækst og forårsager kræft (insertionsmutagenese).
Det samme kunne blandt andet observeres i en Paris-undersøgelse. Efter den første succes viste det sig, at nogle børn, der blev behandlet med genterapi, havde leukæmi. Derudover kan immunsystemet markere de modificerede målceller som fremmede og angribe dem (immunogenicitet).
Endelig, i tilfælde af transduktion med vira, er der en risiko for, at den person, der behandles med genterapi, bliver inficeret med en vild type virus, der bruges som en færge, og at dette vil mobilisere den genetisk modificerede sekvens fra genomet i en sådan grad, at den vil matche den tilsvarende på et uønsket sted Kan integrere konsekvenser.













.jpg)

.jpg)


.jpg)
